OpenEDC Versionen 1.1 – 1.3
Source Data Verification (SDV), Signaturen, Gründe für fehlende Werte und mehr Audits.

Co-Founder / CEO

Heute veröffentlichen wir OpenEDC in der Version 1.3. Damit erfüllen wir alle Anforderung für klinische Studien gemäß der Good Clinical Practice (GCP). Nachfolgend schauen wir uns alle Neuigkeiten seit dem letzten Beitrag im Detail an.
Source Data Verification (SDV)
Source Data Verification (SDV) in klinischen Studien ist ein kritischer Qualitätskontrollprozess, bei dem Daten systematisch überprüft werden, um ihre Genauigkeit, Vollständigkeit und Verlässlichkeit zu gewährleisten. Dies geschieht durch den Abgleich der im Electronic Data Capture (EDC) System dokumentierten Daten mit den ursprünglichen Quelldaten, wie sie in Krankenakten, Laborergebnissen oder anderen Primärdokumenten festgehalten sind. Für die Zulassung neuer Medikamente und Behandlungen stellt der SDV-Prozess daher einen unverzichtbaren Bestandteil der Qualitätssicherung in klinischen Studien dar.
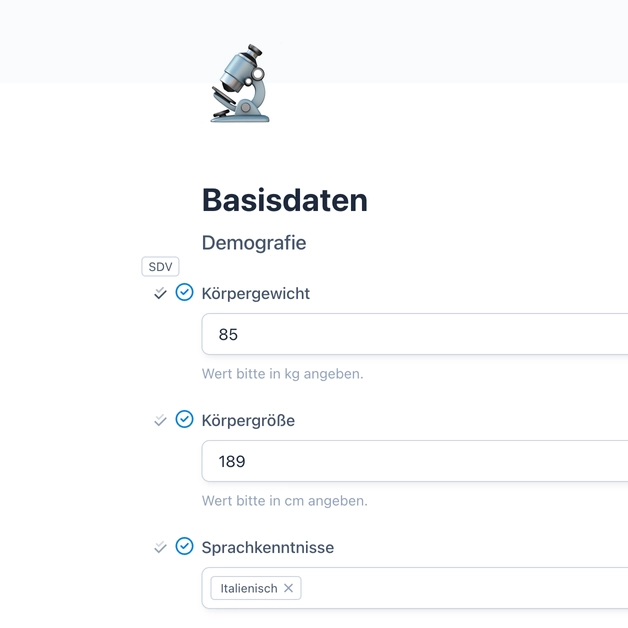
Source Data Verification (SDV) kann in OpenEDC neben jedem Feld durchgeführt werden.
Digitale Signaturen
In klinischen Studien übernimmt die Prüferin oder der Prüfer eine zentrale Rolle bei der Sicherstellung der Datenintegrität und -qualität. Mit einer digitalen Signatur wird dabei die rechtliche Verantwortung für die Korrektheit der erhobenen Daten übernommen. Wichtig dabei ist, dass die oder der Unterzeichnende, sowie das Datum und die Uhrzeit der Signatur eindeutig, zurechenbar und revisionssicher dokumentiert werden. Um sicherzustellen, dass eine unterzeichnende Person wirklich diese Person ist, wird in OpenEDC für jede Signatur eine erneute Authentifizierung vorausgesetzt.
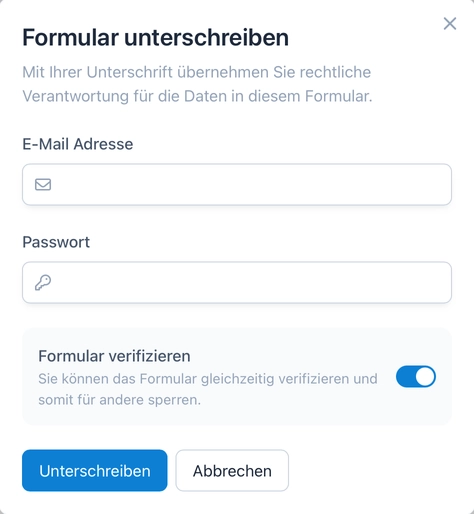
Gemeinsam mit einer Signatur erlaubt es OpenEDC, alle Daten in einem Formular zu verifizieren und somit für eine weitere Bearbeitung zu sperren.
Grund für fehlende Werte
Fehlende Werte sind eine große Herausforderung in der Forschung. Und auch in klinischen Studien sind Datenlücken nicht ungewöhnlich, sei es durch Patientenausfälle, nicht durchgeführte Tests oder fehlende Antworten in Fragebögen. Wichtig ist es jedoch, den Grund für das Fehlen eines Eintrags zu dokumentieren. Das ist jetzt in OpenEDC möglich und orientiert sich an den Null Flavors von HL7 FHIR, die auch in ISO 21090 Anwendung finden. Zu der Angabe eines Grunds kann zusätzlich ein Kommentar angegeben werden, der die Ursache bei Bedarf noch weiter erläutert.
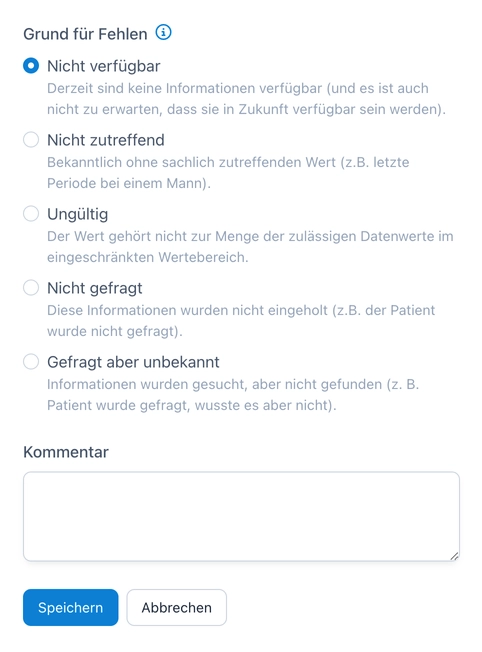
Angabe eines Grundes für fehlende Werte in OpenEDC.
Weitere Neuigkeiten
Weitere Änderungen in den letzten Updates kurz zusammengefasst:
Audit Trail
Der Audit Trail umfasst jetzt auch Änderungen an den Metadaten, also den Formularen. Zusätzlich lassen sich in einer neuen tabellarischen Ansicht alle Änderungen von allen auditierten Daten einsehen.
Rechte auf Formularebene
Lese- und Schreibrechte können jetzt auf Formularebene definiert werden. Somit ist es möglich, dass Nutzende nur bestimmte Formulare sehen oder bearbeiten können.
Dateien in Berichten
Hochgeladene Dateien können jetzt direkt in Bericht angesehen und heruntergeladen werden. Es gibt eine Vorschaufunktion für PDF-, Bild-, und Videodateien.
Damit ist dieser Beitrag beendet. Vielen Dank für Ihr Interesse. Wenn Sie mehr erfahren möchten, vereinbaren Sie eine unverbindliche Demo oder testen Sie unsere App.
